Ранее диентамебу (Dientamoeba fragilis) считали микроорганизмом, принадлежащим к типу Rhizopoda. Организм уникален тем, что существует только в форме трофозоита с двумя ядрами. Этим объясняется ее название – диентамеба. Несмотря на утерю жгута, принадлежность D.fragilis к жгутиковым простейшим подтверждается при электронно-микроскопических исследованиях.
D.fragilis – паразит человека, хотя морфологически сходные паразиты были обнаружены у обезьян в Индии и Панаме. Диентамебы – организмы со значительно варьирующими размерами от 3 до 18 мкм (в среднем 7-12 мкм) Псевдоподии гиалиновые с характерным листовидно зазубренным краем (рис. 92). Движение поступательное, но организмы активны только в свежих пробах фекалий. Вакуоли содержат поглощенных бактерий, которые видны через цитоплазму. У живых трофозоитов ядра не видны. Типичные организмы содержат два ядра, хотя встречаются формы с 3 и 4 ядрами.
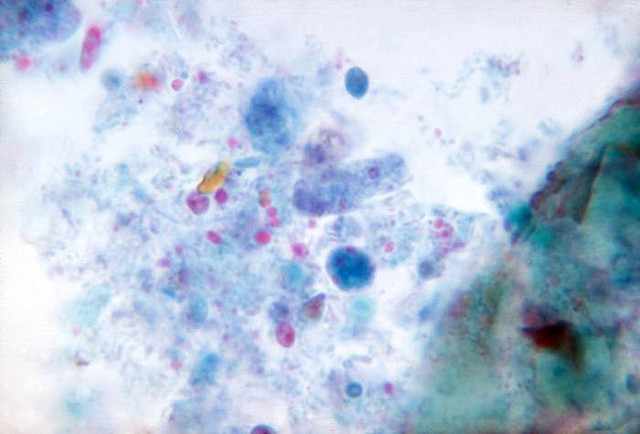
В окрашенных препаратах D.fragilis идентифицируются на основе большой доли (до 80%) бинуклеарных форм с типичной структурой. Ядерная мембрана нежна и не имеет периферического хроматина. В центре ядра лежит большая масса, состоящая из 4-8 отдельных гранул, обычно симметрично организованных.
Диентамеба способна существовать в условиях толстого кишечника на слизистой поверхности крипт – особенно в скоплениях комочков слизи, что и способствует их расселению. Эритроцитов не заглатывает, ткани не инвазирует. В редких случаях легкая слизистая диарея может быть результатом присутствия большого числа паразитов в кишечнике. Выявление неоформленного стула, неопределенных болей, запоров у 15-27% инфицированных иногда относят на счет диентамеб.
Диагноз амебиаза устанавливают на основании данных эпидемиологического анамнеза, клинической картины заболевания и результатов лабораторного исследования.
Решающими для диагноза являются результаты паразитологического исследования. Паразитологический диагноз амебиаза ставят при обнаружении в исследуемом материале тканевой и большой вегетативной формы, трофозоитов-эритрофагов. Материалом для исследования могут служить: фекалии, ректальные мазки, отобранные при ректороманоскопии, биопсийный материал язвенных поражений, аспират содержимого абсцесса печени, причем тканевые формы локализуются в основном в наружных стенках абсцесса, а не в некротических массах, расположенных в центре.
С первого дня болезни проводят микроскопию нативных мазков из свежевыделенного кала в физиологическом растворе и мазков, окрашенных раствором Люголя. При остром и подостром течении заболевания ищут вегетативную тканевую форму амебы, а у реконвалесцентов и бессимптомных носителей малую просветную форму и цисту. Можно готовить также постоянные препараты, окрашенные гематоксилином по Гейденгайну. Выявление только просветных форм и цист амеб в кале недостаточно для окончательного диагноза.
Для повышения эффективности паразитологических исследований применяют многократное (до 3-6 раз) исследование свежевыделенных фекалий (не позднее 10-15 минут после дефекации) и других биологических субстратов, сбор материала в консервирующие жидкости для длительного хранения препарата, методы обогащения.
При наличии клинических признаков кишечного амебиаза и отрицательных результатах паразитологических исследований применяют серологические реакции, основанные на выявлении специфических противоамебных антител. Используется РИФ, РСК, ИФА, реакции торможения гемагглютинации и нейтрализации с парными сыворотками (нарастание титра антител в 4 и более раз). Серологические тесты положительны у 75% больных с кишечным амебиазом и 95% пациентов с внекишечным амебиазом.

Для постановки диагноза внекишечного амебиаза, кроме иммуннологического, проводится комплексное инструментальное обследование: УЗИ, рентгенологическое исследование, компьютерная томография и другие методы, которые позволяют определить локализацию, размеры и число абсцессов, а также контролировать результаты лечения.
Из современных методов иследования используется выявление антигенов дизентерийных амеб в фекалиях и другом материале с помощью моноклональных антител, определение паразитарной ДНК методом ПЦР.
В целом все препараты, используемые для лечения амебиаза можно разделить на 2 группы: контактные или просветные (воздействующие на кишечные просветные формы) и системные тканевые амебоциды.
Для лечения неинвазивного амебиаза (бессимптомных носителей) используют просветные амебоциды. Просветные амебоциды также рекомендуется назначать после завершения лечения тканевыми амебоцидами для элиминации амеб, оставшихся в кишечнике, с целью профилактики рецидивов. В частности имеются наблюдения о развитии амебных абсцессов печени у лиц с кишечным амебиазом, получивших только тканевые амебоциды без последующего назначения просветных амебоцидов. В частности описан рецидив амебного абсцесса печени у больного через 17 лет после успешно излеченного впервые выявленного абсцесса печени.
В условиях, когда невозможно предотвратить повторное заражение, применение просветных амебоцидов нецелесообразно. В этих ситуациях рекомендуется назначать просветные амебоциды только по эпидемиологическим показаниям, например лицам, чья профессиональная деятельность может способствовать заражению других лиц, в частности сотрудникам предприятий питания.
Просветные амебоциды
- Этофамид (Китнос®)
- Клефамид
- Дилоксанид фуроат
- Паромомицин
Для лечения инвазивного амебиаза применяют системные тканевые амебоциды. Препаратами выбора из этой группы являются 5-нитроимидазолы, которые используют как для лечения кишечного амебиаза, так и абсцессов любой локализации.
Системные тканевые амебоциды
5 нитроимидазолы:
- Метронидазол (Трихопол®, Флагил®)
- Тинидазол (Тиниба®, Фасижин®)
- Орнидазол (Тиберал®)
- Секнидазол
Помимо препаратов из группы 5-нитроимидазолов для лечения инвазивного амебиаза и прежде всего амебных абсцессов печени рекомендуется использовать Дегидроэметин дигидрохлорид (в РФ не зарегистрирован) и Хлорохин.
Кишечный амебиаз:
- Метронидазол внутрь 30 мг/кг/сутки в 3 приема в течение 8-10 дней
- или
- Тинидазол до 12 лет 50 мг/кг/сутки (макс. 2г) в 1 прием в течение 3 дней,
- старше 12 лет 2 г/сутки в 1 прием в течение 3 дней
- или
- Орнидазол до 12 лет 40 мг/кг/сутки (макс. 2 г) в 2 приема в течение 3 дней,
- старше 12 лет 2 г/сутки в 2 приема в течение 3 дней
- или
- Секнидазол до 12 лет 30 мг/кг/сутки (макс. 2 г) в 1 прием в течение 3 дней,
- старше 12 лет 2 г/сутки в 1 прием в течение 3 дней
Амебный абсцесс:
- Метронидазол 30 мг/кг/сутки в 3 приема в течение 8-10 дней
- или
- Тинидазол до 12 лет 50 мг/кг/сутки (макс. 2 г) в 1 прием в течение 5-10 дней,
- старше 12 лет 2 г/сутки в 1 прием в течение 5-10 дней
- или
- Орнидазол до 12 лет 40 мг/кг/сутки (макс. 2 г) в 2 приема в течение 5-10 дней,
- старше 12 лет -2 г/сутки в 2 приема в течение 5-10 дней
- или
- Секнидазол до 12 лет 30 мг/кг/сутки (макс. 2 г) в 1 прием в течение 3 дней,
- старше 12 лет 2 г/сутки в 1 прием в течение 3 дней
Альтернативная схема лечения амебного абсцесса:
- Дегидроэметин дигидрохлорид 1 мг/кг/сутки в/м (не более 60 мг) в течение 4-6 дней
- Одновременно или сразу же после завершения курса дегидроэметина при амебных абсцессах печени рекомендуется хлорохин 600 мг основания в сутки в течение 2 дней, затем по 300 мг основания в сутки в течение 2-3 недель
После завершения курса 5-нитроимидазолов или дегидроэметина с целью элиминации оставшихся в кишечнике амеб применяют просветные амебоциды:
- Этофамид 20 мг/кг/сутки в 2 приема в течение 5-7 дней
- Паромомицин -1000 мг/сутки в 2 приема в течение 5-10 дней
В клинически выраженных случаях при соответствующем эпидемиологическом анамнезе, когда в фекалиях обнаруживают большое число непатогенных видов амеб, также рекомендуется проводить лечение амебоцидами, так как в этих случаях высокая вероятность сопутствующей инфекции Е.histolytica.
Неоднородность патологического процесса и клинических проявлений при амебиазе в разных географических регионах, наличие штаммов, Резистентных к стандартным схемам химиотерапии 5-нитроимидазолами, требуют варьирования схем лечения с учетом опыта, накопленного в конкретном районе.
После успешной химиотерапии абсцесса печени остаточные полости обычно исчезают в течение 2-4 месяцев, однако возможна персистенция полостей до 1 года.
Тяжелым больным с амебной дизентерией, вследствие возможной перфорации кишечника и развития перитонита рекомендуется дополнительно назначать антибактериальные препараты, активные в отношении кишечной микрофлоры.
Аспирация (или чрескожное дренирование) рекомендуется при больших размерах абсцесса (более 6 см), локализации абсцесса в левой доле печени или высоко в правой доле печени, сильной боли в животе и напряжении брюшной стенки вследствие возможной угрозы разрыва абсцесса, а также при отсутствии эффекта от химиотерапии в течение 48 часов от ее начала. Аспирация рекомендуется также при абсцессах неясной этиологии. При невозможности закрытого дренажа, разрыве абсцесса и развитии перитонита проводится открытое оперативное лечение.
При назначении кортикостероидов у больных амебиазом могут развиться тяжелые осложнения, вплоть до развития токсического мегаколона. В связи с этим при необходимости лечения кортикостероидами жителей эндемичных зон, у которых высок риск инфицирования Е.histolytica необходимо предварительное обследование на амебиаз. При сомнительных результатах целесообразно превентивное назначение амебоцидов с последующим назначением кортикостероидов.
В настоящее время амебиаз является практически полностью излечиваемым заболеванием при условии ранней диагностики и адекватной терапии.
